پتاسیم کربنات

خواص
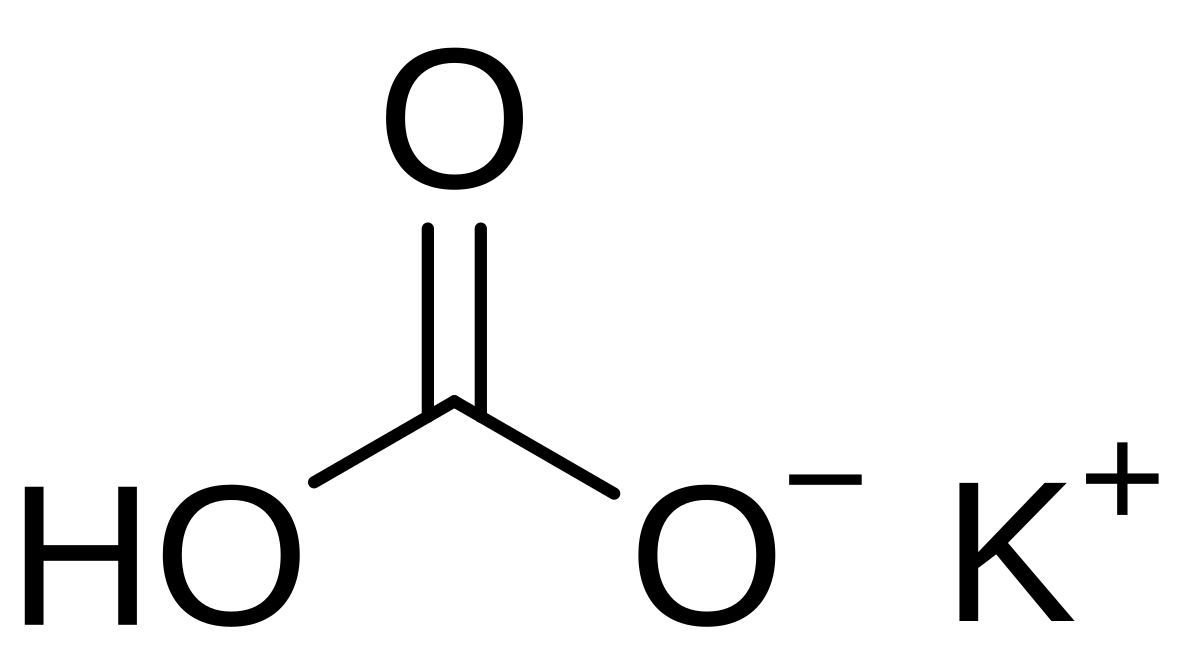
- فرمول شیمیایی K
- 2CO
- 3
- جرم مولی 138.205 گرم در مول
- ظاهر سفید ، جامد رطوبت
- تراکم 2.43 g / cm3
- نقطه ذوب 891 درجه سانتیگراد (1636 درجه فارنهایت ؛ 1،164 کیلوگرم)
- نقطه جوش تجزیه می شود
- حلالیت در آب 112 گرم در 100 میلی لیتر (20 درجه سانتیگراد)
- 61.0 گرم در 100 میلی لیتر (100 درجه سانتیگراد)
- انحلال پذیری
- 3.11 گرم در 100 میلی لیتر (25 درجه سانتیگراد) متانول
- محلول در الکل ، استون است
- حساسیت مغناطیسی (χ) − 59.0 · 10−6 سانتی متر مکعب / مول
- خطرات
- برگه اطلاعات ایمنی ICSC 1588
- نمودارهای GHS GHS07: مضر است
- هشدار کلمه سیگنال GHS
- اظهارات خطر GHS H302 ، H315 ، H319 ، H335
- اظهارات احتیاطی GHS P261 ، P305 + 351 + 338
- NFPA 704 (الماس آتش)
- الماس چهار رنگ NFPA 704
- 010
- نقطه اشتعال غیر قابل اشتعال
- دوز یا غلظت کشنده (LD ، LC):
- LD50 (دوز متوسط) 1870 میلی گرم در کیلوگرم (خوراکی ، موش صحرایی)
- ترکیبات مرتبط
- آنیونهای دیگر بی کربنات پتاسیم
- کاتیونهای دیگر کربنات لیتیوم
- کربنات سدیم
- کربنات روبیدیوم
- کربنات سزیم
- ترکیبات مرتبط کربنات آمونیوم
- به استثنای موارد دیگری که داده شود ، داده ها برای مواد در حالت استاندارد خود (در دمای 25 درجه سانتیگراد [77 درجه فارنهایت] ، 100 کیلو پاسکال) داده می شوند.
پتاسیم کربنات یک ترکیب غیر آلی با فرمول K2CO3 است. این یک نمک سفید است که در آب قابل حل است. دلپذیر است و اغلب به صورت جامد مرطوب یا مرطوب به نظر می رسد. پتاسیم کربنات عمدتا در تولید صابون و شیشه استفاده می شود.
تاریخ
کربنات پتاسیم جز primary اصلی پتاس و خاکستر مروارید یا نمک های تارتار تصفیه شده بیشتر است. از لحاظ تاریخی ، خاکستر مروارید با پخت پتاس در کوره برای از بین بردن ناخالصی ها ایجاد می شد. پودر ریز و سفید باقیمانده خاکستر مروارید بود. اولین اختراع ثبت شده توسط اداره ثبت اختراعات ایالات متحده به دلیل بهبود روش ساخت پتاس و خاکستر مروارید در سال 1790 به ساموئل هاپکینز اعطا شد.
در اواخر قرن 18 آمریکای شمالی ، قبل از تولید بکینگ پودر ، از خاکستر مروارید به عنوان یک عامل خمیرمایه برای تهیه نان های سریع استفاده می شد.

تولید پتاسیم کربنات
کربنات پتاسیم توسط واکنش هیدروکسید پتاسیم با دی اکسید کربن به صورت تجاری تهیه می شود:
2 KOH + CO2 → K2CO3 + H2O
از محلول Sesquihydrate K2CO3 · 3⁄2H2O ("هیدرات پتاس") متبلور می شود. حرارت دادن این جامد بالاتر از 200 درجه سانتیگراد نمک بی آب می دهد. روش جایگزین ، کلرید پتاسیم با دی اکسید کربن در حضور یک آمین آلی تصفیه می شود تا بی کربنات پتاسیم داده شود ، سپس کلسینه می شود:
2 KHCO3 → K2CO3 + H2O + CO2
کاربرد های مهم
(به لحاظ تاریخی) برای تولید صابون ، شیشه و چینی
به عنوان یک ماده خشک کننده خفیف که ممکن است سایر عوامل خشک کننده مانند کلرید کلسیم و سولفات منیزیم ناسازگار باشند. این ماده برای ترکیبات اسیدی مناسب نیست ، اما در صورت داشتن مقدار ناخالصی اسیدی برای خشک کردن یک فاز آلی می تواند مفید باشد. همچنین ممکن است برای خشک کردن بعضی از کتون ها ، الکل ها و آمین ها قبل از تقطیر استفاده شود.
در آشپزی ، جایی که کاربردهای سنتی زیادی دارد. این ماده یک ماده سازنده در تولید ژله چمن ، غذایی است که در غذاهای چینی و آسیای جنوب شرقی مصرف می شود و همچنین رشته فرنگی و کیک ماه چینی که با دست کشیده می شود. این ماده همچنین برای لطیف کردن سه قلو استفاده می شود. در دستورالعمل های نان شیرینی زنجبیلی آلمان اغلب از کربنات پتاسیم به عنوان عامل پخت استفاده می شود ، اگرچه در ترکیب با گاو شیرین است. استفاده از پتاسیم کربنات برای جلوگیری از آسیب باید به مقدار مشخصی محدود شود و نباید بدون راهنما استفاده شود.
در قلیایی سازی پودر کاکائو برای تولید شکلات فرآیند هلندی با ایجاد تعادل در pH (به عنوان مثال ، اسیدیته را کاهش دهید) دانه های طبیعی کاکائو ؛ همچنین عطر را افزایش می دهد. روند افزودن کربنات پتاسیم به پودر کاکائو معمولاً "هلندی کردن" (و فرآورده هایی که به آنها پودر کاکائو فرآوری شده توسط هلند گفته می شود) نامیده می شود ، زیرا این فرآیند برای اولین بار در سال 1828 توسط Coenraad هلندی Johannes van Houten توسعه یافت.
به عنوان یک عامل بافر در تولید میوه یا شراب.
در اسناد عتیقه ، گزارش شده است که برای نرم کردن آب سخت استفاده شده است.
به عنوان مهار کننده آتش در خاموش کردن سرخ کن های چربی و انواع مختلف آتش سوزی های مربوط به گروه B.
در مهار آتش آئروسل متراکم ، اگر چه به عنوان محصول جانبی نیترات پتاسیم.
به عنوان یک عنصر در شارهای جوشکاری ، و در پوشش شار در میله های جوش قوس الکتریکی.
به عنوان یک عنصر خوراک دام برای تأمین نیاز به پتاسیم حیوانات پرورشی مانند پرورش دهندگان مرغ گوشتی.
به عنوان تنظیم کننده اسیدیته در snus سوئدی - سایپرز ، باشگاه دانش
منبع : https://en.wikipedia.org/wiki/Potassium_carbonate
- ۹۹/۰۶/۳۱