اسید اگزالیک
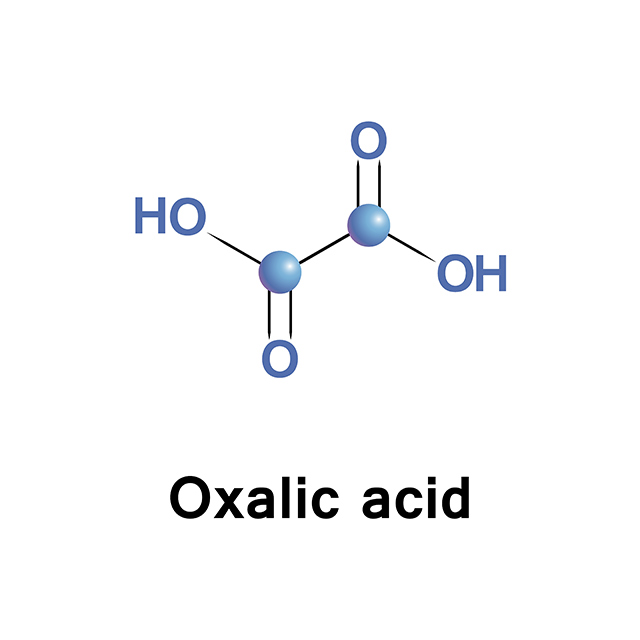
فرمول ساختاری اسید اگزالیک
فرمول اسکلتی اسید اگزالیک
مدل پر کردن فضا اسید اگزالیک
اسید اگزالیک دی هیدرات
نامها
ترجیحی iupac نام
اسید اگزالیک
نام IUPAC سیستماتیک
Ethanedioic اسید
نامهای دیگر
سفید کننده چوب ، اسید خرچنگ
شناسهها
شماره CAS
144-62-7 (بی آب) بررسی
6153-56-6 (دی هیدرات) بررسی
مدل 3D (JSmol)
تصویر تعاملی
3DMet
B00059
بیلشتاین مرجع 385686
چبی
CHEBI: 16995 بررسی
چمبل
Chembl146755 چک
عنکبوت
946 چک
بانک مواد
بررسی db03902
Echa InfoCard 100.005.123 ویرایش این در ویکیداده
شماره EC
205-634-3
مرجع Gmelin 2208
KEGGNAME
C00209 ☒
مش اگزالیک+اسید
PUBCHEM CID
971
شماره RTEC
RO2450000
UNII
9e7r5l6h31 بررسی
0k2l2ij59o (دی هیدرات) بررسی
شماره سازمان ملل 3261
داشبورد CompTox (سازمان حفاظت محیط زیست)
DTXSID0025816 ویرایش این در ویکیداده
اینچی
لبخند
ویژگیها
فرمول شیمیایی C2H2O4
جرم مولی 90.034 g·mol-1
(بی آب)
126.065 g·mol-1 (دی هیدرات)
ظاهر کریستال سفید
بوی بی بو
تراکم 1.90 g * cm-3 (بدون آب ، در 17 °C)
1.653 g·cm-3 (دی هیدرات)
نقطه ذوب 189 به 191 °C (372 به 376 °F ؛ 462 به 464 K)
101.5 °C (214.7 °F ؛ 374.6 K) دی هیدرات
حلالیت در آب 90-100 g / L (20 °C) [2]
حلالیت 237 g / L (15 °C) در اتانول
14 گرم / L (15 °C) در دی اتیل اتر
فشار بخار <0.001 mmHg (20 °C) [4]
اسیدیته (pKa) 1.25, 4.14[5]
هیدروژنوکسالات پایه مزدوج
حساسیت مغناطیسی (x) -60.05·10-6 سانتی متر 3/مول
فارماکولوژی
ATCVET کد QP53AG03 (که)
خطرات
خطرات اصلی خورنده
برگه اطلاعات ایمنی MSDS خارجی
NFPA 704 (آتش الماس)
NFPA 704 چهار رنگ الماس
310سید
نقطه اشتعال 166 °C (331 °F; 439 K)
دوز کشنده یا غلظت (LD، LC):
LDLo (کمترین منتشر شده) 1000 میلی گرم / کیلوگرم (سگ, دهانی)
1400 میلی گرم / کیلوگرم (موش)
7500 میلی گرم / کیلوگرم (موش, دهانی) [6]
NIOSH (محدودیت قرار گرفتن در معرض سلامت ایالات متحده):
PEL (مجاز) TWA 1 میلی گرم/m3[4]
REL (توصیه می شود) TWA 1 میلی گرم/m3 ST 2 میلی گرم/m3[4]
IDLH (خطر فوری) 500 میلی گرم/m3[4]
ترکیبات مرتبط
ترکیبات مرتبط اگزالیل کلرید
اگزالات سدیم
اگزالات کلسیم
فنیل اگزالات استر
مراجع جعبه اطلاعات
اسید اگزالیک یک ترکیب آلی با نام IUPAC ethanedioic acid و فرمول HO است
2C-شرکت
2H. این ساده ترین اسید دی کربوکسیلیک است. این یک جامد کریستالی سفید است که یک محلول بی رنگ در آب تشکیل می دهد. نام آن از این واقعیت است که محققان اولیه اسید اگزالیک جدا شده از گیاهان گلدار از جنس اگزالیس ، معمولا به عنوان چوب sorrels شناخته شده است. این به طور طبیعی در بسیاری از غذاها اتفاق می افتد ، اما مصرف بیش از حد اسید اگزالیک یا تماس طولانی مدت پوست می تواند خطرناک باشد.
اسید اگزالیک استحکام اسید بسیار بیشتر از اسید استیک. این یک عامل کاهش است[7] و پایه مزدوج آن, شناخته شده به عنوان اگزالات (ج
2O2−
4) ، یک عامل کلات کننده برای کاتیون های فلزی است. به طور معمول ، اسید اگزالیک به عنوان دی هیدرات با فرمول C رخ می دهد
2ساعت
2O
4 * 2H2O.
محتویات
1 تاریخچه
2 آماده سازی
2.1 روش های آزمایشگاهی
3 ساختار
4 واکنش
5 وقوع
بیوسنتز 5.1
5.2 وقوع در غذاها و گیاهان
تولید 5.3 توسط قارچ ها
5.4 دیگر
6 بیوشیمی
7 برنامه های کاربردی
7.1 تمیز کردن
7.2 استخراج متالورژی
7.3 استفاده از طاقچه
8 محتوا در مواد غذایی
9 سمیت
10 یادداشت
11 مراجع
12 لینک های خارجی
تاریخچه
تهیه نمکهای اسید اگزالیک (خرچنگ اسید) از گیاهان شناخته شده بود و حداقل پس از 1745 زمانی که گیاه شناس هلندی و پزشک هرمان Boerhaave جداسازی نمک از چوب ترشک. توسط 1773 ، فرانسوا پیر Savary فریبورگ ، سوئیس اسید اگزالیک از نمک خود را در ترشک جدا شده بود.
در سال 1776 سوئدی داروخانه ها Carl Wilhelm Scheele و Torbern اولاف برگمن تولید اگزالیک اسید واکنش با اسید نیتریک غلیظ; Scheele به نام اسید که منجر به socker-syra یا såcker-syra (قند اسید). توسط 1784 ، شیل نشان داده بود که "اسید شکر" و اسید اگزالیک از منابع طبیعی یکسان بودند.
در سال 1824 ، شیمیدان آلمانی فردریش Wöhler اسید اگزالیک با واکنش سیانوژن با آمونیاک در محلول آبی به دست آمده است. این آزمایش ممکن است اولین سنتز یک محصول طبیعی را نشان دهد.
آماده سازی
اسید اگزالیک عمدتا توسط اکسیداسیون کربوهیدرات ها یا گلوکز با استفاده از اسید نیتریک یا هوا در حضور پنتوکسید وانادیوم تولید می شود. انواع پیش سازهای می تواند مورد استفاده قرار گیرد از جمله اسید گلیکولیک و اتیلن گلیکول.[یک روش جدیدتر مستلزم کربنیلاسیون اکسیداتیو از الکل به diesters اسید اگزالیک:
4 ROH + 4 CO + O2 → 2 (CO2R)2 + 2 H2O
این diesters پس از آن به اسید اگزالیک هیدرولیز می شوند. تقریبا 120,000 تن در سال تولید می شود.
از لحاظ تاریخی اسید اگزالیک به طور انحصاری با استفاده از مواد سوزاننده به دست آمد, مانند هیدروکسید سدیم یا پتاسیم, در خاک اره. تجزیه در اثر حرارت از فرمت سدیم (در نهایت از مونوکسید کربن آماده) ، منجر به تشکیل اگزالات سدیم ، به راحتی به اسید اگزالیک تبدیل شده است.
روش های آزمایشگاهی
اگر چه می توان آن را به آسانی خریداری اگزالیک اسید تهیه می شود در آزمایشگاه توسط اکسید کننده ساکارز با استفاده از اسید نیتریک در حضور مقدار کمی از vanadium pentoxide به عنوان یک کاتالیزور است.
جامد هیدراته را می توان با گرما یا تقطیر azeotropic خشک کرد.
توسعه یافته در هلند یک electrocatalysis توسط مجتمع مس کمک می کند تا کاهش دی اکسید کربن به اسید اگزالیک;این تبدیل با استفاده از دی اکسید کربن به عنوان ماده خام برای تولید اسید اگزالیک.
ساختار
اسید اگزالیک بی آب به عنوان دو پلی مورف وجود دارد ؛ در یکی از نتایج پیوند هیدروژن در یک ساختار زنجیره ای مانند در حالی که الگوی پیوند هیدروژن در فرم دیگر یک ساختار ورق مانند تعریف می کند.از آنجا که مواد بی آب هر دو اسیدی و آب دوست (به دنبال آب) است ، آن است که در استری استفاده می شود.
واکنش
واکنش های اسید اگزالیک بسیار هستند.
اسید اگزالیک اسید نسبتا قوی با وجود اینکه اسید کربوکسیلیک است:
C2O4H2 ⇌ C2O4H - + H+ pKa = 1.27
C2O4H - ⇌ C
2O2−
4 + H + pKa = 4.27
اسید اگزالیک بسیاری از واکنش های مشخصه دیگر اسیدهای کربوکسیلیک دستخوش. این استرها مانند دی متیل اگزالات (mp 52.5 به 53.5 °C (126.5 به 128.3 °F)) تشکیل می دهد.[20] آن را به شکل یک کلرید اسید به نام اگزالیل کلرید.
اگزالات ، پایه مزدوج اسید اگزالیک ، یک لیگاند عالی برای یون های فلزی ، به عنوان مثال دارو اگزالیپلاتین است.
اسید اگزالیک و اگزالات را می توان با پرمنگنات در یک واکنش اتوکاتالیستی اکسید کرد.[
مقادیر pKa اسید اگزالیک در ادبیات از 1.25-1.46 و 3.81-4.40 متفاوت است. اد 100 از CRC, در آزاد 2019 دارای ارزش های 1.25 و 3.81.
وقوع
بیوسنتز
حداقل دو مسیر برای تشکیل آنزیم واسطه اگزالات وجود دارد. در یک مسیر ، اگزالواستات، یک جزء از چرخه کربس اسید سیتریک ، به اگزالات و اسید استیک توسط آنزیم اگزالواستاز هیدرولیز:
[O2CC(O)CH2CO2]2 - + H2O → C
2O2−
4 + کانال
3CO−
2 + ساعت+
همچنین از دهیدروژناسیون اسید گلیکولیک ناشی می شود که توسط متابولیسم اتیلن گلیکول تولید می شود.
وقوع در غذاها و گیاهان
اگزالات کلسیم شایع ترین جزء سنگ کلیه است. محققان اولیه اسید اگزالیک جدا شده از چوب ترشک (اگزالیس). اعضای خانواده اسفناج و brassicas (کلم ، کلم بروکلی ، جوانه بروکسل) بالا در اگزالات ، به عنوان ترشک و چتر مانند جعفری.[27] برگ ریواس حاوی حدود 0.5٪ اسید اگزالیک و جک در منبر (Arisaema triphyllum) حاوی کریستال اگزالات کلسیم است. به طور مشابه ، خزنده ویرجینیا ، یک انگور تزئینی رایج ، اسید اگزالیک را در انواع توت ها و همچنین کریستال های اگزالات در sap، به شکل رافید تولید می کند. باکتری ها تولید اگزالات از اکسیداسیون کربوهیدرات.
گیاهان جنس Fenestraria تولید الیاف نوری ساخته شده از اسید اگزالیک کریستالی برای انتقال نور به سایت های فتوسنتز زیرزمینی.
Carambola ، همچنین به عنوان starfruit شناخته می شود ، همچنین حاوی اسید اگزالیک همراه با caramboxin است. آب مرکبات حاوی مقادیر کمی اسید اگزالیک است. مرکبات تولید شده در کشاورزی ارگانیک حاوی اسید اگزالیک کمتر از تولید شده در کشاورزی معمولی است.
شکل گیری طبیعی کلسیم اگزالات patinas در برخی از سنگ آهک و سنگ مرمر و مجسمه ها و بناهای تاریخی مطرح شده ناشی از واکنش های شیمیایی از کربنات سنگ با اگزالیک اسید ترشح شده توسط گلسنگ یا سایر میکروارگانیسم ها.
تولید توسط قارچ ها
بسیاری از خاک قارچ گونه ترشح اسید اگزالیک و در نتیجه بیشتر حلالیت از کاتیونهای فلزی افزایش در دسترس بودن برخی مواد مغذی خاک و می تواند منجر به تشکیل اگزالات کلسیم کریستال.
غیره
قیر اکسید شده یا قیر در معرض اشعه گاما نیز حاوی اسید اگزالیک در میان محصولات تخریب آن است. اسید اگزالیک ممکن است شسته شدن رادیونوکلئید در قیر برای دفع زباله های رادیواکتیو مطبوع را افزایش دهد.
بیوشیمی
پایه مزدوج اسید اگزالیک آنیون هیدروژنوکسالات است ، و پایه مزدوج آن (اگزالات) یک مهار کننده رقابتی آنزیم لاکتات دهیدروژناز (LDH) است. ldh کاتالیز تبدیل پیروات به اسید لاکتیک (محصول نهایی فرآیند تخمیر (بی هوازی)) اکسید کردن کوآنزیم NADH به NAD+ و H+ همزمان. بازگرداندن سطوح nad+ برای ادامه متابولیسم انرژی بی هوازی از طریق گلیکولیز ضروری است. به عنوان سلول های سرطانی ترجیحا با استفاده از متابولیسم غیر هوازی (نگاه کنید به اثر واربورگ) مهار LDH نشان داده شده است به مهار تشکیل تومور و رشد بنابراین جالب بالقوه دوره از درمان سرطان است.
برنامه های کاربردی
حدود 25 درصد از اسید اگزالیک تولید شده به عنوان یک موردانت در فرآیندهای رنگرزی استفاده می شود. همچنین در سفید کننده ها ، به ویژه برای pulpwood ، و برای حذف زنگ و دیگر تمیز کردن ، در بکینگ پودر ،و به عنوان یک معرف سوم در ابزار تجزیه و تحلیل سیلیس استفاده می شود.
تمیز کردن
برنامه های اصلی اسید اگزالیک عبارتند از تمیز کردن یا سفید کردن ، به ویژه برای حذف زنگ (عامل پیچیده آهن). ابزار آن در عوامل حذف زنگ به علت تشکیل یک نمک پایدار و محلول در آب با آهن آهن، یون فریوکسیلات است. محصول تمیز کردن Zud حاوی اسید اگزالیک است.
اسید اگزالیک نیز به طور گسترده ای به عنوان یک سفید کننده چوب استفاده می شود
منبع:
https://en.wikipedia.org/wiki/Oxalic_acid





